信息来源:医学界
Casgevy的获批“打开了门”,但基因编辑和绝大多数疗法不同,它是一针“无法反悔的药”。
在革命性的基因编辑工具CRISPR/Cas9被发明11年后,英国成为了全球首个授予该技术医疗许可的国家。当地时间11月16日,英国药监局 (MHRA)宣布,批准CRISPR/Cas9基因编辑疗法Casgevy上市,用于治疗镰状细胞病(SCD)和输血依赖性β地中海贫血(β地贫)。
“我非常兴奋,有点不知所措。”美国生物学家、加州大学伯克利分校生物学教授詹妮弗·杜德纳第一时间在博客中写道。2012年她发明了该技术的原型,并在2020年斩获诺贝尔化学奖。CRISPR/Cas9基因编辑让科学家能精准地对人类DNA进行改造,一劳永逸抵御基因性疾病。
美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)也将在随后跟进,美国FDA预计将在12月8日做出是否允许上市的裁决。因为涉及伦理、安全性等问题,多年来基因编辑疗法一直受到严格的上市监管。
近年来国内也涌现出不少基因疗法创新企业。在今年5月的2023年全球华人遗传学大会上,中国科学院院士陈润生教授对“医学界”表示:“尤其是在遗传性疾病的诊治中,还有很多没打开的‘窗户’,我国发展新的基因编辑系统,依然有很多原始创新的机会。”
基因编辑疗法Casgevy是什么?
Casgevy疗法由美国生物科技公司CRISPR Therapeutics开发,在2019年首次展开体外试验,提出将利用基因编辑工具,治疗血红蛋白缺陷引起的SCD和β地贫。
根据公司在11月16日的声明,此次获批后,或有2000名英国患者符合Casgevy用药条件。
SCD和β地贫都属于遗传性血液疾病,患者体内红细胞无法正常地携带氧气。前者被视为最常见的严重单基因疾病之一,若缺少医疗护理和社区支持,50%-80%的SCD患儿会在5岁前夭折。后者曾被列入WHO的“危害人类健康的6种常见病”。
目前,SCD和β地贫主要依赖输血等维持治疗,部分患者可以通过造血干细胞移植获得根治,但配型成功率低、费用高、年龄限制是普遍问题。有数据显示,英国SCD和β地贫患者的平均死亡年龄分别为40岁、55岁。
而基于基因编辑工具CRISPR/Cas9系统开发的Casgevy,能在体外改造、修饰患者的自体造血干细胞,恢复能携带氧气的血红蛋白。再输回患者体内,以实现疾病的彻底扭转。
根据MHRA的公告,Casgevy获批上市源于两项临床研究,均达到了临床终点,即减少SCD患者疼痛和血管闭塞性危象,缓解β地贫患者的输血需求。
针对SCD的临床研究共纳入45名受试者。在完成全程疗效观察的29人中,97%(28)的人至少12个月未出现严重疼痛。所有人连续12个月无严重复发性血管闭塞危象。而在β地贫相关研究中,42名受试者提供了可评估数据。其中39人(93%)治疗后的至少12个月内不用再输血。另有3人的输血需求下降70%。
上述研究还显示,Casgevy的安全性良好,不良反应与自体造血干细胞移植基本一致。主要表现为疲劳、发烧、恶心、感染风险增加等。
在今年3月召开的“第三届人类基因组编辑国际峰会”上,首位接受Casgevy治疗的SCD患者维多利亚·格雷(Victoria Gray)做主题演讲。在接受治疗近1年后,她没有做过输血治疗,疼痛几乎消失。骨髓细胞活检显示,超过81%的细胞产生了预期的遗传变化。这说明基因编辑治疗在其体内持续生效。
目前,药物研发方没有公布Casgevy售价。2022年8月,美国食药监局(FDA)批准基因疗法Zynteglo用于治疗β地贫,定价为280万美元(约合人民币2028万元)。按此推算,Casgevy大概率也是“天价药”。
基因编辑十年
“这是里程碑式的时刻,基因编辑的发展让遗传性罕见病、各类慢病等的治愈看到希望。”中国科学院神经科学研究所研究员杨辉告诉“医学界”。
2012年,CRISPR/Cas9发明者詹妮弗·杜德纳首次在《科学》杂志发布了体外基因编辑的结果。研究一开始并没有引发关注,她认为这和文章标题“适应性细菌免疫中可编程、双RNA引导的DNA核酸内切酶”有关。不少人不明白到底是在说什么。
但这不妨碍CRISPR随后成为现代生物学中最著名的发明之一。在2020年的诺贝尔奖颁奖现场,委员会评价道,“这是一项划时代的实验”。
CRISPR的灵感来源于细菌。上世纪80年代,科学家发现细菌体内有一段特殊的DNA片段,它最终会转录翻译成一种类似“剪刀”作用的蛋白质,切掉病毒的基因防止被入侵。詹妮弗·杜德纳受到了启发,创造出了能精准切割、粘贴人类基因的CRISPR/Cas9。
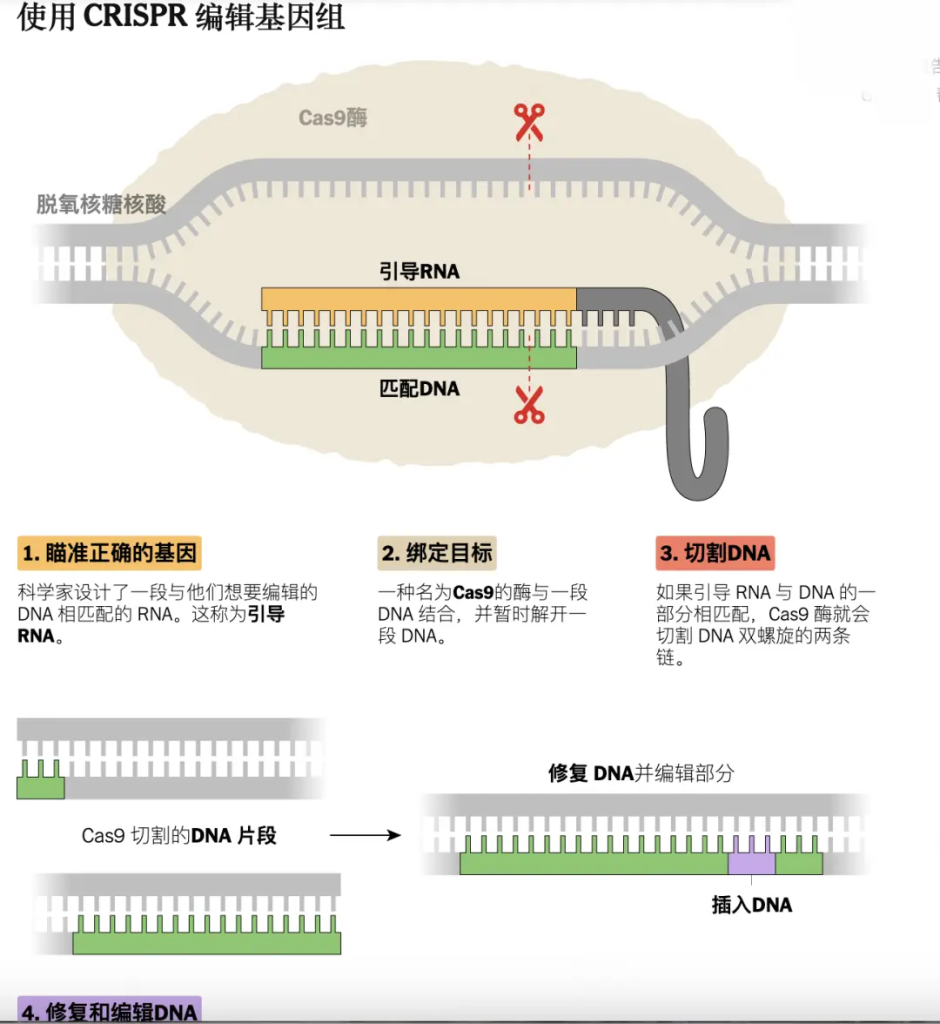
CRISPR基因编辑工作原理
短短十余年间,这项技术迅速改变了人类研究和治疗疾病的方式。癌症学家用其来精准研究肿瘤的基因靶点,慢病专家希望能一次性改变基因,避免患者终身服药。植物学家也开始对农作物进行改造,试图培育出更富含营养的产品。
虽然看似科幻,“它离我们并不遥远。从新技术出现到获批上市只用了约十年,非常迅速了。”杨辉对“医学界”表示。而CRISPR/Cas9也只是基因编辑的其中一种工具,除了本次获批的Casgevy,全球还有大量不同技术路线的管线在研发之中。
“根据不同的递送载体和编辑方式,基因编辑疗法覆盖的病种也不同。”杨辉说,因新冠mRNA疫苗迅猛发展的脂质纳米颗粒LNP递送系统精确瞄准在肝脏;病毒载体AAV递送则通向全身,杨辉团队尝试用它治疗视网膜疾病。
CRISPR有时会产生错误的基因修饰,造成无法挽回的后果。华裔科学家刘如谦从2016年起相继开发了“碱基编辑”和“先导编辑”,被称为CRISPR2.0版本,它能在不断裂DNA双链的情况下实现单个遗传字母互换,因此更加精准与安全。
2022年,美国一家药企宣布完成碱基编辑疗法VERVE-101全球首次给药,通过修改基因降低胆固醇”,号称将一针永久预防心血管疾病。“碱基编辑解决了初代CRISPR 的部分安全性问题。”正序生物首席执行官牟晓盾告诉“医学界”,“此外慢病往往由多种因素叠加,碱基编辑还可以进行多靶点编辑,也分担了脱靶的风险。”
在慢病领域的尝试,反映了科学家试图在基因编辑前景的探索上再迈一步。毕竟相比无药可治的罕见疾病,多数慢病已有高性价比的成熟疗法,审批机构对基因编辑的疗效和安全性也将提出更高要求。
“技术在不断革新,但无法笼统地去评价它是否安全。这需要不同研究方向的科学家在实验中不断发现问题,更新策略。”杨辉说。
CRISPR发展得如此迅速,也让法规的制定和伦理共识显得滞后,2018年的“基因编辑婴儿事件”一度让行业蒙上阴影。今年年初,英国的一个公民陪审团又发布了一份报告,敦促英国政府考虑修改法律,允许科学家在疾病“最早期”,即人类胚胎时就进行基因编辑。该陪审团由受遗传病影响的人组成,有些是死于遗传病孩子的父母。
包括脱靶效应、效率问题、免疫排斥和片段丢失等技术难点,Casgevy的获批“打开了门”,但基因编辑和绝大多数疗法不同,它是一针“无法反悔的药”。
“鉴于这项技术只有10年历史,已经是非凡的进步。但使用这样强大的技术,需要迎接对于责任的挑战。”詹妮弗·杜德纳在年初的人类基因组编辑国际峰会上表示。
国内的进展如何?
数据显示,2016年我国基因治疗市场规模仅约为0.15亿元,但随着近年来基因治疗临床试验的大量开展、以及相关利好产业政策的支持等,2021年已快速上升至2.7亿元左右,2027年预计将达到约500亿元。
陈润生院士对“医学界”表示,基因编辑是一个系统,其中的CRISPR/Cas9发展最早,可能最为成熟,“我国的基础研究也一直在不断探索,从基因编辑总体系统的设计,到具体工作的蛋白,包括应用到不同病种,都有原始创新的机会。”
“之前是专利权被国外垄断,包括递送平台等技术都存在限制。现在这些问题差不多打破了。”杨辉介绍,由于专利保护,在Cas9以及Cas9依赖的基因编辑工具上,国内企业已没有太多空间。而将方向瞄准在Cas13系统,2022年1月,杨辉所在的辉大基因团队开发的Cas13X和Cas13Y工具,获得美国专利局授权。
另一本土基因编辑疗法初创公司正序生物,孵化自上海科技大学,其科学创始人团队开发了变形式碱基编辑系统tBE,这也是首个获海外专利授权的本土自研碱基编辑工具。据了解,正序生物据此开发的针对β-地中海贫血症创新碱基编辑疗法,在10余位健康者和患者捐献的造血干细胞中完成有效性和安全性的观察,在动物模型中有超过6个月的安全性验证和疗效观察。
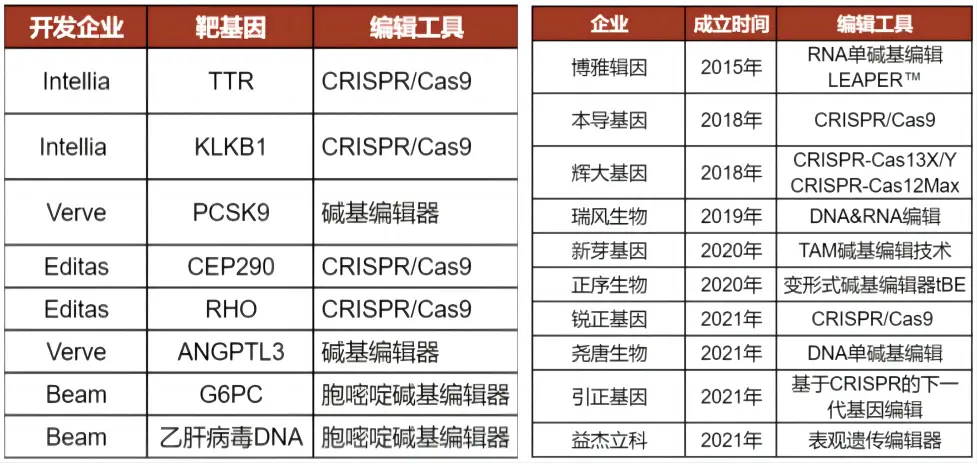
据不完全统计,截至2021年国内至少有10家企业开发了基因编辑系统。“本土企业的机会在于,除了像Cas9这类早期技术手段,在‘新型工具’上和海外几乎处于同一起跑线,应该把势头保持下去。当然一些细节的技术难点,涉及多学科,还需要更底层的基础研究和创新技术去解决,有差距但并没想象得那么大,有些细分领域国内甚至领先。”牟晓盾说。
杨辉则认为挑战还在于适应证的选择,“要么在靶点上做出差异化,要么同样的靶点比海外推得更快,疗效和安全性更好。”
“过去常见的是海外先做出有临床效果的疗法,国内创新企业跟着‘Fast Follow’。但以后会越来越少,投资人也更加理性,这种方式很难融到资金。”杨辉说,在基因编辑领域,依靠基础研究上的本土创新,以及大量国内患者数据,“去拓展国外进度较慢、或还未涉及的管线,在某个适应证上拿到全球首个数据,这才是发展方向。”
更重要的是,基因编辑并不是单纯在彼此间比较,临床的疗法选择也不是“越先进越好”,包括卫生经济学等的考量,陈润生院士表示,“基因编辑技术主要是为了改变在遗传密码水平上,一些影响健康或导致疾病的变异,精准定位是它独到性的优势。
“但我认为它也只是整个医学发展中的一种方法。比方说现在的小分子药、免疫疗法、以及小核酸药物等,已经对很多疾病的治疗起到了重要作用。基因编辑应该是和其他方法相辅相成,协同治愈疾病。”陈润生院士说。









